 Может случиться, что теплоты сгорания А и В неодинаковы. Пусть, например. А имеет теплоту сгорания на 100 калорий большую, чем В. Значит, при переходе А в В должно выделиться 100 калорий, чтобы был соблюден закон сохранения энергии. Если мы создадим такие условия, что имеющиеся частицы, сгруппировавшись, могут дать тело А или тело В, то преимущественно будет образовываться тело В потому что его внутренняя энергия на 100 калорий (на 1 г) меньше, чем энергия А, а это и значит, что В явится более устойчивой формой, чем А.
Может случиться, что теплоты сгорания А и В неодинаковы. Пусть, например. А имеет теплоту сгорания на 100 калорий большую, чем В. Значит, при переходе А в В должно выделиться 100 калорий, чтобы был соблюден закон сохранения энергии. Если мы создадим такие условия, что имеющиеся частицы, сгруппировавшись, могут дать тело А или тело В, то преимущественно будет образовываться тело В потому что его внутренняя энергия на 100 калорий (на 1 г) меньше, чем энергия А, а это и значит, что В явится более устойчивой формой, чем А.
Так же обстоит дело и с кристаллическими состояниями углерода. Нернст в 1911 г. и Рот в 1915 г. нашли, что при комнатной температуре и атмосферном давлении теплота сгорания алмаза на 450 калорий превышает теплоту сгорания графита. Это значит, что при переходе алмаза в графит (практически это осуществимо) выделяется 450 калорий (на 1 г алмаза) и что при комнатной температуре и нормальном давлении графит является более устойчивым состоянием углерода, чем алмаз. Практически это значит, что мало вероятно, чтобы при низких температурах и давлениях алмаз было бы легче получить, чем графит.
 Однако при высоких давлениях и температурах, как показали расчеты, можно достичь того, что теплота сгорания графита будет выше теплоты сгорания алмаза, а значит последний явится более устойчивым по сравнению с графитом.
Однако при высоких давлениях и температурах, как показали расчеты, можно достичь того, что теплота сгорания графита будет выше теплоты сгорания алмаза, а значит последний явится более устойчивым по сравнению с графитом.
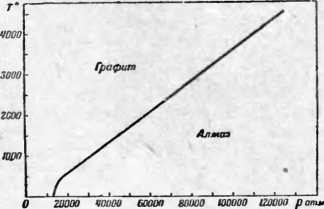
Приводимая диаграмма показывает, что в области высоких давлений и сравнительно низких температур преимущественно устойчив алмаз, в случае же высоких температур и повышенных давлений более устойчив графит. Устойчивость обоих одинакова, если брать давления и температуры в точках кривой, изображенной на диаграмме и делящей ее на две части. Это будет переходным случаем.
Трудность заключается не только в создании условий, в которых устойчив алмаз, но и в самом механизме кристаллизации того или иного продукта, или, как говорят, в кинетике этого процесса. Кристалл может образоваться как из отдельных атомов углерода, которые, присоединяясь, будут надстраивать кристалл, так и из обломков другой кристаллической решётки которая была разрушена на мелкие части, но не на отдельные атомы. Такие части уже неспособны разрушиться до атомов в процессе кристаллизации и будут соединяться с обломками старой кристаллической решётки, причем внутренняя энергия не сможет тут дойти до минимума, соответствующего устойчивому состоянию; это может иметь место только тогда, когда движутся отдельные атомы, которые способны перераспределиться и при этом принять наивыгоднейшее расположение.
Такая структура, построенная из обломков решёток и не являющаяся устойчивой в термодинамическом смысле, вместе с тем будет достаточно стойкой. Для перевода ее в более устойчивую форму (в смысле минимума внутренней энергии) требуется расшатать решётку и раскачать входящие в нее атомы, а на обычном языке это значит — нагреть ее, или подвергнуть сильному сжатию, или сделать и то и другое вместе.
Эти соображения позволяют надеяться на получение алмаза и в той области температур и давлений, где более устойчивым является графит. Только при этом придется применить температуры, при которых кристаллы графита еще не полностью разрушаются, а в то же время алмаз уже способен перестраиваться и образовывать присущую ему решётку.
Вообще же замечено, что с точки зрения кинетики (т. е. механизма образования кристаллов углерода) графит стоит в более выгодном положении. Это. очевидно и объясняет все или почти все неудачи производившихся до сих пор опытов получения искусственных алмазов.
Интересная задача выделения химически чистого углерода в форме алмаза еще не решена, но можно надеяться, что она будет решена в недалеком будущем. Основная трудность заключается в умелом подборе условий, удовлетворяющих как термодинамическим. так и кинетическим требованиям. На языке практики это означает необходимость получать высокие (до 60—70 тыс. ат) давления совместно с высокими температурами и накопить большой опытный материал, касающийся поведения различных форм углерода при разных условиях (определение теплоты сгорания, изучение механизма кристаллизации и т. д.).
Далее из категории История технологий: "Колумб, Коперник или всё-таки Лука Пачоли? Бухгалтерия знает всё"







